已有的研究表明,蛙类歪头病的致病因子为细菌,目前已经从各类病蛙中鉴定出十几株病原菌,包括:米尔伊丽莎白菌(Elizabethkingia miricola)、脑膜脓毒性伊丽莎白菌(E. meningoseptica)、肺炎克雷伯菌(Klebsiella pneumoniae)、醋酸钙不动杆菌(Acinetohacter calcoaceticus)等,并以伊丽莎白菌属最为常见。这些菌株多为多重耐药菌,其中一些菌株(如米尔伊丽莎白菌)与人类临床分离株(可引起新生儿脑膜炎)具有较高的亲缘关系。当前,虽然对于歪头病致病因子的鉴定工作取得了一定进展,但其病理机制却极少有研究,且我们对于健康蛙类所携带的本底病原菌的丰度及其潜在感染途径等均不了解,这些研究的空缺使得养殖蛙类歪头病 的防治工作迟迟无法取得进展。
的防治工作迟迟无法取得进展。
为此,中国科学院成都生物研究所江建平研究团队的朱未、常利明和赵春霖调查了四川境内养殖黑斑蛙(俗称青蛙)的歪头病爆发情况。发现疾病爆发的蛙场内至少存在两种类型的病蛙:其中一种仅表现出歪头的症状,其运动平衡丧失,大量溺死;另一种同时表现出歪头、白内障和浮肿等症状,继而于阴暗处病死(图1)。通过比较无症状个体、歪头个体和“歪头+白内障”个体的脑、眼球和消化道菌群发现,米尔伊丽莎白菌是这些病蛙的致病因子,其在两种病蛙的脑中均具有很高的丰度,而仅在“歪头+白内障”个体的眼球中具有高丰度。所有个体的消化道菌群中米尔伊丽莎白菌的丰度极低,说明其从消化道感染黑斑蛙的可能性较低。值得注意的是,多种其他类型的歪头病致病菌亦存在于养殖黑斑蛙的体表或肠道中,虽然其不是此次疾病爆发的致病因子,但是却有引起歪头病爆发的潜在可能。
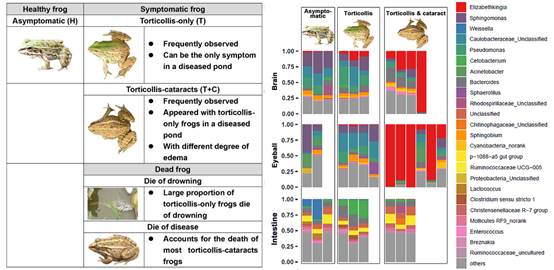
图1 不同症状的病蛙和微生物组成分析
组织病理学分析发现,歪头个体表现出明显的脑膜血管充血,而“歪头+白内障”个体还额外表现出明显的软脑膜淋巴细胞渗透以及中枢神经系统损伤;两种病蛙均出现肝脏脂肪储备降低的现象。病蛙与无症状个体的主要基因表达差异存在于脑组织中,且这些差异基因主参与免疫反应,病蛙表现出免疫识别(NOD-like receptor signaling pathway and Toll-like receptor signaling pathway)、发炎反应(TNF signaling pathway and Cytokine-cytokine interaction)和适应性免疫应答(B cell receptor signaling pathway)的全面激活。两类病蛙的基因表达在脑组织和肝脏中存在明显差异。在脑组织中,“歪头+白内障”个体表现出强烈的天然免疫和炎症应答,且急性期蛋白的转录水平显著升高;在肝脏中,“歪头+白内障”个体同样表现出更显著的急性期蛋白表达上调和能量代谢基因下调。这些结果共同提示两种病蛙处于脑部感染的不同病理阶段。结合人细菌性脑膜炎的病程,我们推测歪头个体处于软脑膜侵入和感染的早期,还未引发脑膜炎;由于未发现歪头个体的肌肉存在明显的病理和基因转录变化,因此我们推测歪头症状和运动失衡可能是源于神经系统感染。而在“歪头+白内障”个体中,感染已经引起脑膜炎,其所伴随的系统性发炎可导致“血眼屏障”的突破(眼部感染)和组织水肿,进而解释了为何“白内障”症状的出现可以预测脑膜炎的发生(图2)。
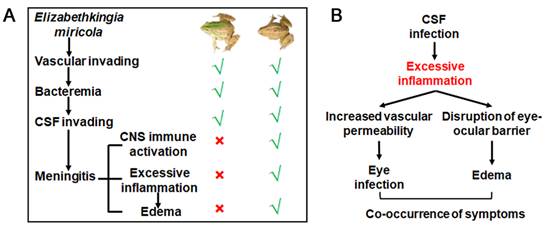
图2 典型症状的病理机制
基于这些结果,我们为歪头病的预防提出以下几点建议:
1.出现歪头症状时病原菌已入侵脑膜,抗生素治疗所导致的细菌裂解可能促进炎症反应,加速病蛙的死亡,因此该疾病应以预防为主;
2.由于多种致病菌被黑斑蛙正常携带,监测黑斑蛙体表及养殖环境的微生物组成和丰度或可预测歪头病暴发的风险;
3.有研究表明两栖动物在暴露于某些灭活的病原物之后仍可获得免疫记忆,而伊丽莎白菌感染可激活黑斑蛙的适应性免疫,我们或可尝试使用灭活病原菌暴露的方式提前激活黑斑蛙对该病原菌的的免疫能力。
该研究得到了中国科学院战略先导研究项目(XDA19050201), 国家自然科学基金项目(31900327), 中国科学院西部之光人才培养项目(2016XBZG_XBQNXZ_B_008), 以及四川省科技厅基础条件平台建设项目(2019JDPT0020)的支助。近日,这项工作以常利明为第一作者,题为 “Microbiomic and transcriptomic insight into the pathogenesis of meningitis-like disease in cultured Pelophylax nigromaculatus”发表于水产领域经典期刊Aquaculture。
