8月19日,中国科学院成都生物研究所生物资源利用中心王飞研究团队联合四川大学化学学院冯小明院士和董顺喜教授团队在药物化学国际顶级期刊Journal of Medicinal Chemistry上发表题为“Discovery of a Covalent Inhibitor of Pro-Caspase-1 Zymogen Blocking NLRP3 Inflammasome Activation and Pyroptosis”(文章链接)的最新研究成果,报道了化合物CIB-1476共价结合pro-caspase-1抑制NLRP3炎症小体的激活和细胞焦亡。
Caspases是一类结构相关的半胱氨酸蛋白酶家族,是细胞死亡和天然免疫的关键调节蛋白。炎症小体激活后,caspases家族会在天冬氨酸残基上被底物切割,产生活性剪切体,导致炎症因子如IL-1β和IL-18的释放和细胞死亡。根据其细胞功能,可分为凋亡caspases (caspase -2、-3、-6、-7、-8、-9和-10) 和炎症caspases (caspase -1、-4、-5和-11)。在人类细胞的胞质浓度下,caspases以未加工的失活状态的原酶形式(zymogen)存在,从而作为一种天然的保护机制控制可导致细胞死亡的原酶激活。目前开发caspase蛋白家族的选择性抑制剂非常具有挑战性,因为它们具有共同的底物要求和类似的亚基构型。因此,靶向caspase原酶是实现对特定caspase选择性的一种潜在方法,因为caspase原酶在其家族成员中可能存在更大的差异。
NAIP/NLRC4,NLRP3/6/7和AIM2/IHI16等多种炎症小体的激活导致了一个共同的下游事件:caspase-1的激活。过去针对caspase-1抑制剂的开发,主要是针对其催化区以四肽底物作为抑制剂,它们仅在caspase-1二聚化形成活性位点后才能关闭蛋白酶活性。然而,抑制caspase-1活性位点终止炎症信号提供治疗益处的机会有限,因为在免疫细胞(如巨噬细胞)中caspase-1 在炎症小体组装后就迅速失活。这也是传统的caspase-1抑制剂,如pralnacasan、emricasan和belnacasan (VX-765),由于副作用或疗效问题而在临床阶段被停止开发的主要原因。因此,在caspase-1自激活之前,通过靶向无酶活性的caspase-1原酶(pro-caspase-1)发现新的非肽类抑制剂,可以为治疗caspase-1相关疾病如痛风、关节炎、老年痴呆等提供新的途径,但是该工作尚存在巨大的技术挑战,因为无酶活性的pro-caspase-1缺乏传统的可被化学小分子靶向的口袋结构。
王飞研究员团队通过针对caspase-1的高通量筛选,发现前期冯小明院士团队合成的一类环己烯基异硫氰酸酯类化合物(Angew. Chem. Int. Ed. 2018. 57,9113-9116)具有良好的抑制caspase-1活性的作用。其中化合物CIB-1476表现出最优的caspase-1抑制活性(IC50 ~ 0.65 µM)。初步的构效关系研究表明,CIB-1476的骨架结构和异硫氰酸酯共价基团的位置共同决定了该类化合物的caspase-1 抑制活性。CIB-1476能够特异性抑制caspase-1的活性,而对caspase-3、-4、-5、-7、-11没有影响;有效的抑制NLRP3和AIM2炎症小体的组装和激活,从而抑制炎症因子IL-1β的释放以及gasdermin D (GSDMD)介导的细胞焦亡。通过蛋白质质谱、生物素探针和点突变等手段,作者发现CIB-1476能够不可逆的共价结合pro-caspase-1原酶中的Cys285位点(位于活性催化区)以及Cys397位点(位于底物识别和变构区),在对酶活性依赖性的IL-1β的释放以及非酶活性调控的NF-κB活化方面表现出比VX-765更持久的抗炎作用。化学蛋白质组学分析也显示CIB-1476与细胞内caspase-1结合。并且CIB-1476也在小鼠体内表现出良好的安全性和一定的代谢稳定性,可以通过抑制小鼠体内NLRP3炎性体的激活显示出有效的抗急性痛风和腹膜炎作用,而在Casp1-/-基因敲除小鼠中这种作用则被消除。该研究填补了国际上pro-caspase-1小分子抑制剂的空白,克服了同时使 caspase-1 的酶活性和非酶功能失活的难题,从而为靶向caspase家族原酶的药物研发提供了一种新策略,同时也为开发治疗急性痛风等first-in-class药物开辟了新的途径。
王飞研究员、冯小明教授和董顺喜教授为本论文共同通讯作者;成都生物所曹东怡和席芮颖博士及四川大学李宏业博士为本文并列第一作者。该研究得到了国家自然科学基金、中国科学院战略生物资源计划和中国科学院成都生物研究所攻关团队项目等的支持。
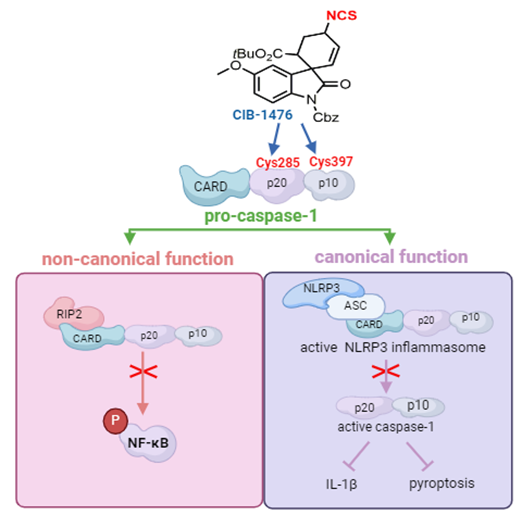
图. CIB-1476的作用示意图
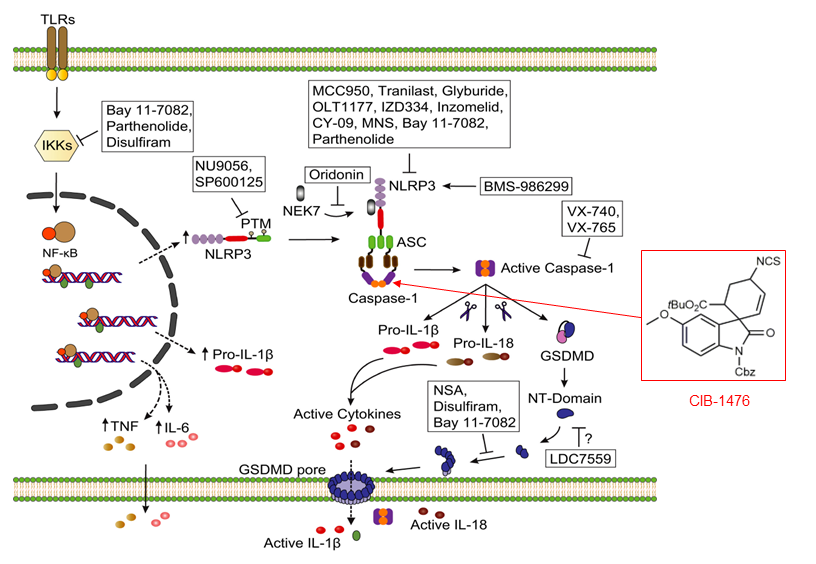
Therapeutic modulation of inflammasome pathways. Immunological Reviews 2020,297:123-138.
